PD-L1为肿瘤细胞提供直接的分子保护,避免了细胞毒性T淋巴细胞 (CTL) 的损害,从而逃避免疫监控。阻断PD-L1可以重新激活和扩大肿瘤反应性CTL,提高免疫治疗的疗效。基于免疫检查点阻断的组合疗法在恶性肿瘤治疗中展现出极大的应用前景,对PD-L1调控网络的解析为开发联合治疗策略提供重要见解。
针对这一需求,近日,来自暨南大学生命科学技术学院张志毅教授课题组在Journal of Proteome Research上发表了题为“Pan-Cancer Proteomics Analysis Reveals Wiskott−Aldrich Syndrome Protein as a Potential Regulator of Programmed Death-Ligand 1”的研究论文。研究针对52例泛癌组织样本的蛋白质表达全景构建共表达网络,识别出与PD-L1表达高度相关的共表达模块和hub基因WASP,提示WASP可能参与PD-L1的表达调控,并在验证队列中获得一致的结果。进一步的体外实验表明,WASP对癌细胞系的PD-L1转录水平具有显著影响。此外,研究还鉴定了WASP对肿瘤免疫微环境的调节效应。结果表明,在WASP累积的背景中存在更高的抑制性淋巴细胞(Foxp3+T细胞, M2型巨噬细胞)浸润密度和免疫检查点(PD1, CTLA4, TIGIT, TIM3)的阳性表达比例,指示了免疫抑制性的分子特征。
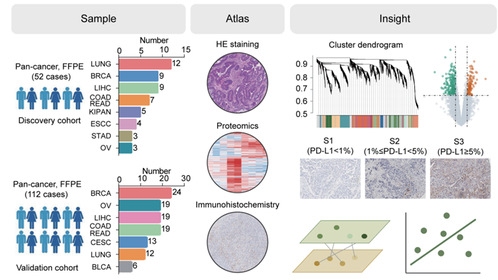
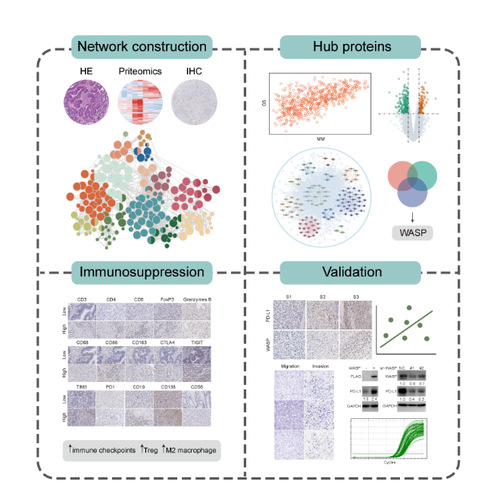
总之,该研究鉴定了WASP作为PD-L1的潜在调控蛋白,WASP/PD-L1信号轴参与调节肿瘤免疫逃避的进程,为癌症免疫治疗的开发提供新的范式。
原文链接:https://pubs.acs.org/doi/10.1021/acs.jproteome.4c00124

